신비한 원소 사전-⑫
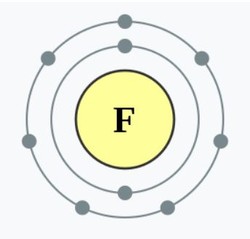
플루오린은 반응성이 매우 큰 원소이다. 불소라고도 부르는데, 불소와 수소가 결합해서 만들어지는 물질이 불산(HF)이다. pH농도가 낮지만 인체에는 3대 강산(염산, 황산, 질산) 이상으로 위험하다.
불산이 피부에 닿을 경우 크기가 작은 불산 분자가 피부로 흡수된다. 흡수된 불산 일부는 인체의 수분과 수소결합을 하며 플루오린 이온이 생성된다.
플루오르 이온은 강한 반응성으로 파고들어 칼슘, 마그네슘 이온과 반응해 전해질 이상을 일으키고 뼈 속 골수조직까지 침투해 뼈를 녹인다.
불산 기체가 호흡기로 들어오면 몸속 장기를 녹이기 시작한다. 반응성과 독성이 강한 플루오린을 분리해내는 데 많은 어려움이 따랐다. 플루오린 분리를 위해 희생한 과학자를 ‘플루오린 순교자’라고 불릴 정도였으니 그만큼 어려웠고 값진 일이었다.
플루오린 분리에 성공하여 1906년 노벨화학상을 받은 무아상(Henri Moissan)은 실험 과정에서 한쪽 눈을 잃었다.

플루오린화합물이 사용되는 대표적인 분야가 치아 관련 분야이다. 산(aicd)으로부터 치아를 보호하는 효과가 있어 치약에도 들어가고, 수돗물에도 플루오린을 첨가해 충치를 예방하는 사업이 전개되기도 한다.
그 외에 프레온가스의 형태로 에어컨 등의 냉매로 사용되거나, 들러붙지 않는 프라이팬의 재료로 사용되기도 했으나 유해성 문제가 계속 불거지고 있다.

불산은 특히 산화규소 물질을 잘 녹여내는데, 바로 유리 물질이다. 휴대전화를 포함한 모바일 기기는 갈수록 진화한다. 많은 정보를 다루기 위해 화면은 커지는데, 화면을 보호하는 유리는 강하면서도 얇고 가벼워야 한다.
불산은 이 강화유리를 연마하는 데에도 사용하고, 규소를 기반으로 하는 반도체 공정에서도 효율 좋은 식각제로 사용한다.

