신비한 원소 사전-⑥
|
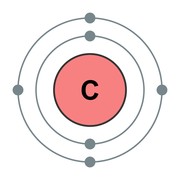
C |
6 |
원자가전자 : 4 |
원자량 : 12.01g/mol |
|
전자배열 : [He]2s22p2 |
|||
|
carbon |
탄소 |
비금속 |
|
이 결합에 참여하지 않은 전자 하나는 그래핀 평면에서 자유전자처럼 남아있다. 그래핀이 철보다 강한 이유는 평면에 펼쳐진 육각형 구조 때문이고 전기가 잘 통하는 이유는 결합에 참여하지 않은 전자 때문이다.
이런 그래핀이 모여 마치 페이스트리 빵처럼 겹겹이 결합한 것이 흑연이다. 각각의 그래핀 층끼리는 약하게 붙어 있다. 층 방향으로는 잘 깨진다는 것이다. 종이에 연필로 글을 쓰는 것은 손의 압력으로 흑연에서 그래핀 덩어리를 층의 결 방향으로 깨뜨려 종이 섬유질 틈에 붙이는 원리다. 물론 종이에 붙어 있는 물질은 그래핀 한 층이 아니라 수천, 수백만 층이 붙은 작은 흑연이다.
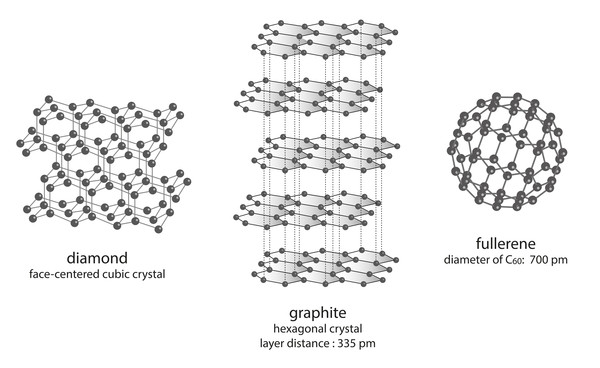
탄소의 존재가 알려지기 이전부터 탄소동소체인 흑연, 목탄, 다이아몬드 등은 줄곧 이용되었다. 무정형 탄소동소체인 목탄이나 숯은 금속의 제련에 중히 쓰였다. 지금은 그 외에도 그래핀, 풀러렌 등 다양한 동소체가 있다는 것이 알려졌다. 워낙 흔히 쓰이는 만큼, 탄소의 최초 발견자에 대해서는 논란이 많다. 학계에 남은 최초의 보고는 1752년 영국의 조지프 블랙이다.

1772년 라부아지에A. Lavoisier가 같은 무게의 숯과 다이아몬드를 태웠을 때 같은 양의 이산화탄소가 발생한다는 것을 발견하고, 다이아몬드와 숯이 같은 원소로 만들어진 동소체임 을 밝혔다. 1789년 자신의 저서에서 탄소를 원소로 규정하고, 목탄을 의미하는 라틴어 carbo에서 따온 carbon이라는 이름을 붙였다.

탄소는 일부 무기물을 제외하고 대부분의 물질에 들어 있다. 생명체를 비롯한 온갖 유기물이 탄소로 이루어져 있는 것이다. 광합성과 호흡의 과정에서 에너지가 생성되고 소비된다. 지구상에서 일어나는 탄소의 순환으로 생태계가 작동된다고 해도 과언이 아니다.
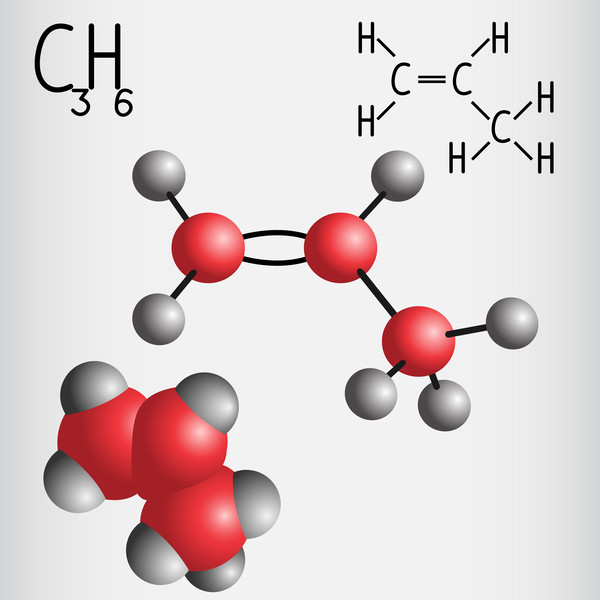
탄소의 가장 큰 특징은 다른 탄소원자와 다양한 공유결합을 한다는 것이다. 단일, 이중, 심지어 삼중결합까지 한다. 이런 특징은 다른 원소에서 찾아보기 힘들다. 이런 까닭에 탄소가 분자의 뼈대를 이룬다. 탄소의 독특한 결합능력 때문에 현재 조사된 것만 해도 탄소화합물의 수가 천만 종 가까이 된다. 탄소를 제외한 다른 모든 원소의 화합물을 합한 것보다 더 많은 수다.

탄소 자체는 위험성이 없는 원소이다. 하지만 인류가 화석연료를 사용하면서 대기 중에 이산화탄소를 배출하는데, 이것이 지구온난화의 원인이 되어 기후 위기로 지구 생태계를 위협한다. 이산화탄소를 없애기 어려운 이유는 결합력이 크기 때문에 분해를 위해서 다른 에너지가 필요하고 그 만큼 이산화탄소를 발생하기 때문이다.

